В чем особенность строения молекулы воды
Из всех соединений водорода наибольшее значение имеет его оксид Н2O, называемый водой. Общее количество воды на Земле, включая связанную в минералах литосферы и мантии, оценивается в 1,6 · 1010 км3, в том числе пресной воды — 9 • 107 км.Вода-непременный участник всех процессов жизнедеятельности. В живых организмах она составляет от 50 до 90 % их общей массы.Пресная вода содержит от 0,05 до 1 г/л растворенных солей. Самые важные из них — гидрокарбонаты магния и кальция, присутствие которых делает воду жесткой.
Океанская вода содержит в среднем 35 г/л растворенных солей. В основном это хлористый натрий NaCl (27 г/л). Установлено, что океанская вода содержит в той или иной форме практически все элементы периодической системы.
Изолированная молекула воды имеет уголковое строение.
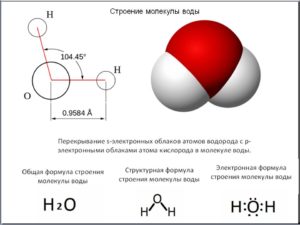
Атом кислорода находится в состоянии sр3-гибридизации. Две орбитали идут на образование связей с водородом, на двух других располагаются неподеленные пары. Такое строение выделяет воду из всех соединений, в которых существуют водородные связи. Только в воде число протонов равно числу неподеленных пар, и поэтому только в воде осуществляется объемная система водородных связей. Идеальный кристалл оксида водорода -льда — подобен кристаллу алмаза. Существенно, что при плавлении кристалла разрушается только 15 % всех водородных связей и в жидкой воде структурные фрагменты льда сохраняются вплоть до температуры кипения. Этим объясняется увеличение плотности воды при плавлении, большая теплота испарения, а значит, и высокая температура кипения воды. Лишь в газовой фазе вода практически не ассоциирована.
 Наличие неподеленных пар на атоме кислорода, большой дипольный момент, •Удобная• геометрия делают воду весьма реакционноспособным веществом. Она реагирует со многими простыми веществами, как металлами, так и неметаллами, с оксидами, галогенидами и другими классами веществ.
Наличие неподеленных пар на атоме кислорода, большой дипольный момент, •Удобная• геометрия делают воду весьма реакционноспособным веществом. Она реагирует со многими простыми веществами, как металлами, так и неметаллами, с оксидами, галогенидами и другими классами веществ.
Вода легко входит во внутреннюю сферу комплексных соединений, выступая в роли лиганда. В частности, многие гидратированные катионы переходят из растворов в кристаллы солей, образуя кристаллоГИдРаты.
Наконец, вода является прекрасным катализатором большинства окислительно-восстановительных реакций.