Ионная связь природа связанных химических элементов.
Ионная, или электростатическая связь образуется в случае полного переноса связывающих электронов к более электроотрицательному атому, который становится в результате этого отрицательным ионом — анионом с зарядом, равным количеству перенесенных электронов.
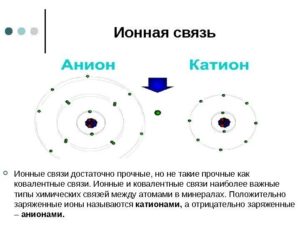
Менее электроотрицательный атом теряет соответствующее количество электронов и становится положительным ионом — катионом. По существу, это предельный случай полярной ковалентной связи, который может реализоваться лишь при взаимодействии атомов, очень сильно отличающихся по электроотрицательности, например в LiF, CaF2, ВаО. Однако, строго говоря, даже в таких соединениях электроны не полностью переходят с катионов на
анионы, а некоторая часть электронной плотности остается делокализованной между ними. Такую связь правильнее рассматривать как преимущественно ионную с малой примесью ковалентности. Ионная связь имеет
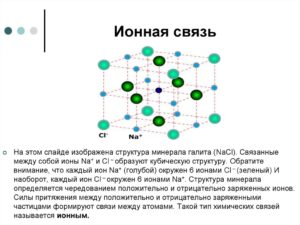
электростатическую природу; это значит, что она не имеет определенного направления в пространстве и ионные соединения не состоят из отдельных молекул, а образуют трехмерные пространственные кристаллические структуры, в которых соотношение между количеством катионов и анионов определяется их зарядами, а взаимное расположение — соотношением радиусов. Энергия ионной связи может быть легко рассчитана по закону Кулона, если известны заряды и радиусы ионов и тип кристаллической решетки.